#背景知识# 所谓 Her-2: EGFR 家族包括人类表皮生长因子受体(human epidermal growth factor receptor, Her)主要分为 Her-1、Her-2、Her-3 和 Her-4 四大成员,其中 Her-2 为胃癌主要的靶点,Her-2 是 EGFR 家族中唯一没有直接配体的受体,在胃癌细胞扩增的比例约为 4%~44%。
胃癌分子靶向治疗的四个进展阶段
ToGA 时代: 发掘出 Her-2 靶点的临床价值后,认为其作为一个有价值基因,由此研发的曲妥珠单抗,利用曲妥珠单抗联合化疗治疗晚期胃癌,结果 OS 较对照组延长 2.8 个月,PFS 延长 1.2 个月,且均有统计学意义,死亡率降落 26% 。应用 Her-2 靶向药曲妥珠单抗治疗有效且安全。
TCGA 时代 :基于 TCGA(癌症基因组图谱,the cancer genome atlas)数据库,胃癌分四型: CIN (Intestinal histology;TP53 突变;RTK-RAS 激活)、 GS (Diffuse histology;CDH1、RHOA 突变;CLDN18-ARHGAP 融合;细胞黏附)、 MSI (Hypermutation;Gastric-CIMP;MLH1 剪切;Mitotic 通路)、 EBV (PIK3CA 突变;PD-L1/2 过表达;EBV-CIMP;CDKN2A 剪切;immune cell signalling)。基于每个分型的不同特点,研发出相关的靶向治疗方案。
ICIs 时代: 免疫检查点*制剂抑**(immunological checkpoint inhibitors,ICIs), 其中主要的两个免疫检查点分别是 细胞毒性 T 淋巴细胞蛋白 4 (CTLA-4)和 PD-1/PD-L1、PD-L2 通路 。研究者意识到肿瘤微环境会有更多更复杂的免疫抑制情况的出现,由肿瘤标志物扩展到肿瘤微环境的标志物。由此开展了 CheckMate649 和 ATTRACTION-4 两个多中心随机临床实验。
Pan-Tumor 时代: 由于胃癌具有较强的异质性,肿瘤微环境具有多样性,要求我们对胃癌的分子机制有更加深入的了解。当前胃癌的分子机制进入多靶点时代,同一环境中,有很多基因发生过表达,导致不同的靶点产生并可能有协同影响,以及局部微环境的改变。在这个时代,我们对肿瘤的认识更加深入,也更加复杂。
究竟什么是 Her-2 阴性胃癌患者,如何定义
张教授认为, Her-2 阳性,是指 Her2 强阳性,不单指 Her2 基因的过表达,还包含基因突变、DNA 的改变等 。 Her2 阴性指不包括任何 Her2 相关基因的改变,含有过表达、突变、基因扩增等, 也有研究者认为 Her-2 低表达也可归为此类 ,对 Her-2 阴性的认识,不能过于局限。Her-2 阴性范围较大也较多,主要含有 EGFR、FGGR、CLDN、MET、DDR、Trop2 ……

从 Her2(-)四个典型的标志物进行描述:
C-MET
MET 表达后结合膜表面蛋白、激活驱动下游表达,主要的四种激活机制是 MET 基因扩增、HGF 自分泌成环、MET 突变、MET 融合 。c-Met 在胃癌组织中有较高的表达率,且往往提示肿瘤具有更高的侵袭性和转移能力,高表达者预后更差。高扩增 Met 基因后,应用沃利替尼能获得生存时间延长,证实是有效的。亦有研究证实非小细胞肺癌高表达 Met 应用沃利替尼治疗后也可以获得生存期延长。

VIKTORY 研究
2019 年,韩国研究者发表的大型伞式研究。该研究纳入 772 例晚期胃癌患者接受高通量测序,其中有 14.7% 的患者接受了标志物指导的治疗。研究结果显示, MET 扩增的发生率为 3.5%,沃利替尼单药治疗 MET 扩增患者的 ORR 为 50%,MET 拷贝数高者的疗效更佳 。
FGFRi
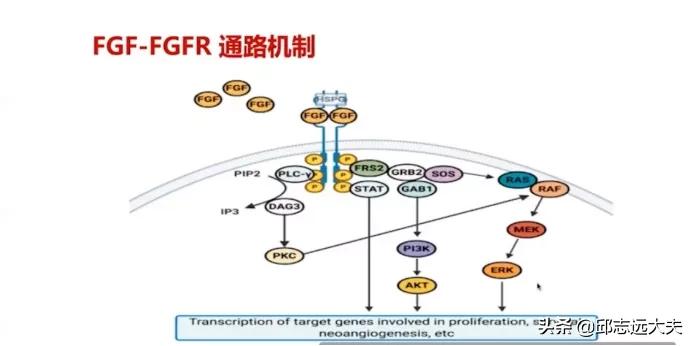
成纤维细胞生长因子受体 2b(FGFR2b)是 FGFR 家(FGFR1-4)的一员,是 FGFR2 的剪接异构体,约 3-61% 的胃癌患者存在 FGFR2b 过表达,FGFR2b 过表达比例取决于肿瘤分期和检测。FGFR 酪氨酸激酶*制剂抑**在 FGFR 突变、融合或易位的肿瘤中显示出临床疗效,其具体的作用机制见上图,FGF 与 FGFR 结合后激活下游通路。
Bemarituzumab 是一种针对 FGFR2b 受体的特异性 IgG1 抗体,Bemarituzumab 选择性地与 FGFR2b 结合,抑制配体结合,介导抗体依赖性细胞介导的细胞毒作用。相关的 II 期临床试验已获得成功,但 III 期临床试验的结果尚未发表。
FIGHT 研究
Bemarituzumab(bema)联合 mFOLFOX6 对比安慰剂联合 mFOLFOX6 一线治疗晚期胃/胃食管交界癌的随机双盲研究。
FIGHT 试验是第一个针对靶向 FGFR2b 过表达的胃/胃食管腺癌的前瞻性随机 II 期研究 ;该研究通过中心实验室进行 IHC 检测,发现一线晚期非 HER2 阳性胃癌/胃食管交界处腺癌中 FGFR2b 阳性的患者约占 30%;Bemarituzumab 与 mFOLFOX6 化疗联合应用,实验组和对照组的 PFS 分别为 9.5 个月和 7.4 个月(P = 0.0727),同时次要起点 OS、ORR 均体现了优势,同时认为 Bemarituzumab 能够在标准化疗基础上进一步提高疗效,改善患者生存。
HRR and HRD
同源重组修复通路基因(HRR)包含有 BRCA1/2,及其上下游调控的众多基因,都是在 DNA 双链断裂的修复中起到重要作用;同源重组修复缺陷(HRD),指的是当 DNA 出现双链断裂时,细胞失去了通过同源重组的方式对断裂进行修复的能力。
DNA 双链断裂进行复制的过程中,发生损伤后,PARP 对其进行检测,在 HRR 机制下,可修复 DNA 进而形成正常细胞,倘若在 HRD 下,由于缺失有效的 HRR 通路,导致修复无效,细胞异常增殖表达,但是在 Olaparib 辅助下,能使异常细胞死亡,从而抑制肿瘤细胞的产生(具体机制见下图)。

GOLD 研究
随机双盲安慰剂对照 III 期临床研究,入组 18 岁以上亚裔晚期胃癌患者,一线化疗后或期间疾病进展,随机分组分别接受口服 Olaparib (100 mg bid) + 紫杉醇 (80 mg/m2 iv) 或安慰剂 + 紫杉醇治疗。 Olaparib 在卵巢癌中被批准的适应症是 BRAC1/2 突变的卵巢癌,由于胃癌领域 BRAC1/2 的突变率太低,所以在入组人群中选择了 ATM 阴性或者是总人群。
这个研究总的结果虽然是阴性的,但是基于 Olaparib 是作用于 DNA 修复途径,所以在未来可能还是会去尝试将其运用在对铂类治疗敏感的患者或者维持治疗等方面,这也是基于对其作用机制的探讨以及 GOLD 研究只是统计学的 P>0.025 的一点点差异而言。 总体来说,OS 延长 2 个月还是一个比较大的进步。
CLDN18.2
表达于正常胃黏膜的紧密连接蛋白,参与构成细胞间的紧密连接,影响细胞离子通道。 CLDN18.2 在胃癌中阳性率可达 40% 左右,其表达特异性使其成为胃癌治疗的潜在靶点。 靶向 CLDN18.2 的抗体药 IMAB362 联合化疗可显著延长 CLDN18.2 阳性胃癌患者生存。

关于进行靶向 CLDN18.2 单抗-IMAB362 的 II 期临床试验,MONO 研究证实单药 IMAB362 治疗复发或难治型进展期胃腺癌或低位食管癌结果显示,其疗效与 CLDN18.2 表达呈正相关。
FAST 研究
IMAB362(剂量为 800 mg/m2)联合化疗(EOX: 表柔比星+奥沙利铂+卡培他滨) ,研究共纳人 161 例患者 (IHC:CLDN18.2 表达强度 >2+, 表达细胞占比 ≥ 50%),其中 CLDN18.2 表达程度 (IHC:CLDN18.2 表达强度 ≥ 2+,表达细胞占比 ≥ 70%),人群疗效更为显著(PFS:6.1 个月 vs. 9.1 个月;OS:9.3 个月 vs 16.6 个月)。作为一线治疗方案可显著延长进展期胃及胃食管结合部肿瘤患者生存,结果显示 PFS 分别为 5.7 个月 vs.7.9 个月 , OS 分别为 8.7 个月 vs. 12.5 个月 。
总结与反思
我们未来将要迈进肿瘤的多靶点时代,由 Her2 时代跨越到超 Her2 时代,这期间伴随着广大研究者的积极推动。
在临床实践中,未来更需要明确肿瘤负荷的主要相关因素,肿瘤生存期间靶点重头产生还是既往就存在,最主要的驱动基因,以及靶点的判断:有几个靶点,哪些有作用,有没有相应的靶向药物,联合治疗方案的有无,基因和免疫组化检测的不同时机,如何确认疗效,如何判断治疗时机及副作用判定标准及处置原则。
未来已来,将至已至,唯变不变,我们唯有时刻能保持一个积极接受新事物,学习新事物的心,精准合理的联合治疗才是克服胃癌的王道。