肿瘤瞭望消化时讯 ioncologyGI
根据GLOBOCAN的数据,2018年,结直肠癌(CRC)是全球第三大最常见的恶性肿瘤,死亡率位列第二,占所有新发肿瘤病例的10.2%,占所有癌症死亡病例的9.2%。过去30年中,CRC发病率在50岁以下的人群中尤其增加,主要是直肠癌增加。酒精、*草烟**、超重和肥胖、加工肉类、高脂肪饮食和缺乏体育活动以及遗传是CRC发生的主要危险因素。多个预测生物标志物可以帮助医生制定转移性CRC治疗决策,例如KRAS、NRAS、BRAF、突变态势、肿瘤位于左侧还是右侧、MSI等。其中,MSI在局部CRC的发生率高达15%~20%。在MSI-H的CRC的治疗中,免疫疗法具有重要的作用。本文重点探讨了近年来免疫疗法在MSI CRC中应用的证据。
20世纪80年代,由于抗蠕虫的左旋咪唑的免疫调节作用,其被首个用于CRC的免疫治疗。其后,5-FU和亚叶酸钙取而代之,迅速成为标准的化疗方案的骨干。随着现代免疫疗法的出现,研究人员开始评估PD-1药物在CRC二线或三线环境中的作用。表1中总结了免疫检查点*制剂抑**(ICIs)相关的试验。
表1. 大多数晚期CRC二线治疗环境下与ICIs相关的研究
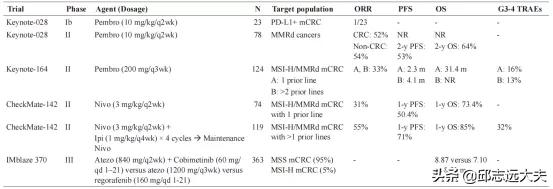
1. 晚期CRC的二线及二线以上免疫治疗
Keynote-028 Ⅰb期试验评估了帕博利珠单抗10 mg/kg持续治疗2年或直至疾病进展或毒性不可接受的安全性和初步疗效,该研究队列包括137例PD-L1+实体瘤患者中的23例晚期CRC患者。中位随访5.3个月后,65%的患者病情进展,唯一的CRC应答者为MSI-H。最常见的AEs为疲劳(13%)、口腔炎(9%)和乏力(9%)。
Le等假设由于错配修复缺陷(MMRd)而导致的高突变和新抗原负担可能受益于ICIs治疗,因此设计了Ⅱ期试验来评估帕博利珠单抗10 mg/kg/q2wk在MMRd mCRC中的抗肿瘤活性,结果显示,免疫相关的客观缓解率(ORR)和20周后的PFS分别达到40%和78%,而在18例MMRp CRC患者中,则仅分别为0%和11%。MMRp mCRC的中位PFS和总生存期(OS)分别为2.2和5.0个月,而MMRd mCRC没有达到这一水平,显示死亡的 HR 为0.22( P =0.05),疾病进展的 HR 为0.10( P <0.001)。9例MMRd非CRC患者中,免疫治疗相关ORR和20周的PFS分别达到71%和67%。有趣的是,MMRd肿瘤中平均1782个突变,而MMRp肿瘤中平均有73个突变( P =0.007)。
随访12.5个月之后,Le等更新了研究,报道了78例不同MMRd肿瘤类型的患者的结果,其中32例证实为种系MMRd肿瘤,另外7例患者有与Lynch综合征一致的家族史。ORR达到53%,疾病控制率(DCR)达到77%,达到任何缓解的平均时间为21周,达到完全缓解的平均时间为42周。CRC和非CRC的ORR相似(52% vs. 54%),Lynch综合征相关和非Lynch综合征相关癌症的ORR相似(46% vs. 59%, P =0.27)。虽然中位PFS和OS未达到,但估计的1年PFS和OS分别为64%和76%,2年的PFS和OS分别为53%和64%。在11例完全缓解和7例部分缓解的患者中,以及帕博利珠单抗治疗2年后停止治疗的患者中,在治疗8.3个月和7.6个月随访时均未视察到肿瘤进展。研究人员未发现应答者和非应答者之间TMB的差异。有趣的是,在确定了7个新抗原反应性T细胞受体在外周血中存在非常低的滴度(<0.02%)后,他们视察到其中4个在应用帕博利珠单抗后迅速增加,然后仅在放射学反应前降落。
在Ⅱ期KEYNOTE-164试验中,Le等评估了帕博利珠单抗200 mg q3wk在124例接受≥2线既往标准治疗(队列A;N=61)或≥1个治疗(队列B;N=63)的MSI-H/MMRd CRC患者中的安全性和活性。ORR(主要起点)在两组中均为33%,两组中均未达到中位缓解持续时间(DOR)。队列A和队列B的中位随访时间分别为31.3个月和24.2个月,队列A的中位PFS和OS分别为2.3个月和31.4个月,队列B的中位PFS和OS分别为4.1个月和未达到。毒性可管理,且与既往试验的报道相比,未出现新的安全性信号。3~4级治疗相关AEs(TRAEs)在队列A和队列B中分别为16%和13%。
2017年,Overmann等在CheckMate-142试验中评估了纳武利尤单抗3mg /kg q2wk在74例≥1线治疗后进展的MSI-H/MMRd mCRC患者中的抗肿瘤活性和安全性。ORR为31.1%,12周DCR为68.9%。中位随访12个月后,中位DOR未达到,1年PFS和OS分别为50.4%和73.4%。根据PD-L1表达或Lynch综合征的临床史,ORR或12周DCR没有差异。
2018年,Overmann等发表了来自CheckMate-142研究的纳武利尤单抗+伊匹木单抗队列的数据。研究人员在119例≥1线全身治疗后进展的MSI-H/MMRd mCRC的患者中评估了上述组合(纳武利尤单抗1 mg/kg + 伊匹木单抗3 mg/kg q3wk,4个剂量,随后纳武利尤单抗3 mg/kg q2wk)的有效性和安全性。ORR和DCR分别为55%和80%。中位DOR未达到,1年PFS和OS分别达到71%和85%。值得关注的是,治疗与症状、角色功能和生活质量的显著改善相关。与其他癌症类型相比,32%的患者发生3~4级TRAEs,且没有新的安全性信号。
此外,IMblaze 370试验是一项开放标签、Ⅲ期试验,363例患者以2:1:1随机接受阿替利珠单抗(840 mg IV q2wk)+cobimetinib(60 mg口服 qd,第1~21天,28天为一个周期)、阿替利珠单抗单药(1200 mg IV q3wk),或者瑞戈非尼治疗(160 mg 口服 qd,第1~21天,每28天为一周期)。值得关注的是,MSI-H患者数量被限制在入组患者的5%。三个研究组中位OS为无差异,因此在未选择的mCRC人群中,该试验未达到其主要起点。
其他研究也在评估二线环境下ICIs单药或联合其他ICIs、细胞毒性化疗以及靶向治疗的作用(表2)。
表2. 大多数正在进行的ICIs在晚期和早期CRC中的相关试验

2. 晚期CRC一线免疫治疗
许多试验研究了ICIs在未选择的生物标志物mCRC一线环境中的活性。然而,如二线环境所示,在这些试验中,ICIs没有达到主要起点,因为大多数患者有MSS mCRC。另一方面,一些试验已经证明了ICIs在一线MSI-H/MMRd mCRC中的有效性和安全性(表3)。 CheckMate-142研究 的另一个队列,研究人员在45例MSI-H/MMRd mCRC患者中评估了纳武利尤单抗+低剂量伊匹木单抗治疗的疗效。ORR和DCR分别为60%和84%,中位随访19.9个月后,1年的PFS和OS分别为77%和83%。20%的患者发生3~4级trae,因此导致11%的患者停止治疗。研究提示,该联合方案具有强大和持久的临床益处,以及可管理的安全性。上述研究结果于2020年ASCO GI上公布。因而,在这种情况下,特别是高肿瘤负荷、需要肿瘤反应的患者中,该联合方案可作为一种有潜力的新标准。 KEYNOTE-177研究 是一项Ⅲ期、开放标签试验,307例MSI-H/MMRd mCRC患者随机接受帕博利珠单抗200 mg q3wk或基于5-FU的化疗联合或不联合贝伐珠单抗或西妥昔单抗q2w。疾病进展后,允许化疗组患者交叉至帕博利珠单抗治疗。中位随访32.4个月后,与化疗相比,帕博利珠单抗治疗的PFS更长(16.5个月 vs. 8.2个月; HR =0.60;95%CI:0.45~0.80; P =0.0002)。OS结果尚不成熟。帕博利珠单抗组的ORR达到43.8%,化疗组为33.1%。在2年时,帕博利珠单抗组83%的患者和化疗组35%的患者仍持续缓解。毒性方面,帕博利珠单抗组的TRAEs率为22%,化疗组为66%。有趣的是,在PFS方面,所有亚组都从帕博利珠单抗获益。然而,KRAS/NRAS突变亚组获得的益处比较少,这一结果值得在进一步的临床试验中得到证实。尽管OS结果仍悬而未决,但考虑到潜在的交叉效应(截至数据分析时,化疗组中59%的患者在试验内或试验外已交叉使用了PD-1/PD-L1药物),因此, KEYNOTE-177试验可以说是一项改变实践的试验,其结果可能确立帕博利珠单抗作为MSI-H/MMRd CRC的新一线治疗标准。
3. FDA批准的适应证和以患者为中心的使用建议
KEYNOTE-028试验的结果以及CheckMate-142试验两个队列的结果,导致FDA批准了帕博利珠单抗(2017年5月)和纳武利尤单抗(2017年8月)以及纳武利尤单抗联合低剂量伊匹木单抗(2018年7月)用于MSI-H/MMRd mCRC的二线治疗。最近,上述方案也得到EMA的批准。 虽然目前还没有比较帕博利珠单抗和纳武利尤单抗或纳武利尤单抗联合伊匹木单抗的试验,但两种抗PD-1药物在ORR、DOR、PFS和OS方面的疗效似乎具有可比性。虽然纳武利尤单抗联合伊匹木单抗的ORR(55%)高于纳武利尤单抗单药(31%)或帕博利珠单抗单药(32%),但PD-1/抗CTLA4联合治疗的毒性也更大,3~4级TRAE几乎翻倍。因此,与其他作者一样,Motta R等建议在ECOG PS良好(0~1)、高肿瘤负荷或优先考虑ORR的快速进展的肿瘤患者中使用纳武利尤单抗联合伊匹木单抗治疗。另一方面,在低肿瘤负荷或由于年龄、共病或ECOG PFS 2的脆弱患者中,需更谨慎的使用抗PD-1药物单药治疗,因为单药比抗PD-1/抗CTLA4的联合更安全。尽管只有一些试验评估了抗PD-1药物一线治疗的有效性和安全性,但必须关注的是, KEYNOTE-177试验中,帕博利珠单抗组的PFS是化疗组的2倍(16.5个月 vs. 8.2个月),而帕博利珠单抗组的ORR达到43.1%(而化疗组为31%)。FDA于2020年6月、EMA于2021年1月分别批准帕博利珠单抗用于MSI-H/MMRd CRC的一线治疗。 在CheckMate-142试验中,纳武利尤单抗/伊匹木单抗组全达到60%的ORR,但导致11%的患者因毒性而停止治疗。因此,关于PD-1单抗单一疗法或抗PD-1/抗CTLA4组合的选择,我们相信在二线环境下给出的建议,同样适用于一线环境下。KEYNOTE-177试验的亚组分析中,KRAS/NRAS突变的患者并未从帕博利珠单抗治疗中获益。这一结果值得在特定的前瞻性试验中进行评估。最后,必须指出的是,KEYNOTE-177的OS结果在本文发表时仍不成熟,因此,我们应该等待最终的OS分析,以及正在进行的试验的结果,以给出明确的建议。因此, 所有的晚期结肠癌患者必须评估KRAS、NRAS、BRAF、HER2和MSI。如果肿瘤显示高MSI(MSI-H),免疫治疗是治疗的选择。 如果治疗的目的是达到高缓解率,且患者ECOG PS为0~1,无相关共病,为非老年患者(>70岁),则应考虑纳武利尤单抗/伊匹木单抗联合治疗。如果患者的肿瘤负担较低,因而高缓解率的相关性较低,或者患者有有限的共病或者ECOG PS 2,抗PD-1单药治疗应该是治疗的选择。针对MSI-H/MMRd mCRC的免疫治疗选择,同样的考虑也适用于一线和二线。
4.CRC中的免疫治疗耐药
虽然免疫治疗已被证明是一种新的治疗选择,但免疫治疗的耐药标志物已经在实体肿瘤患者中被发现,已有JAK1/2、IFNGR1/2和IRF1118的报告,尤其是JAK1和JAK2。JAK1或JAK2的失活突变会导致获得性以及原发性的对抗PD-1治疗的耐药。B2M的截断突变会导致MHC Ⅰ类抗原呈递受损,产生无法引起T细胞反应的免疫逃逸变异。肿瘤中染色质重塑复合物(PBRM1、ARID2和BRD7)的稳定性有助于免疫治疗耐药,这使得DNA修复过程中无法招募MMR基因,并随后减少新抗原的负载。此外,免疫编辑已被报道是耐药性的一种机制。免疫编辑表明,免疫系统和癌细胞之间的持续相互作用导致肿瘤内缺乏新抗原表达的亚克隆的选择,导致免疫原性差和对免疫治疗的耐药性。CRC免疫治疗耐药的机制尚不清楚,需要进一步的研究来确认这一问题。
5.未来展望
随着最近免疫疗法在MSI-H人群的获批,免疫治疗领域正在迅速发展。然而,许多问题仍悬而未决。大多数CRC患者(MSS患者)不能从目前获益的免疫治疗中获益。因此,有多项正在进行的研究正在评估不同免疫治疗模式(包括PD-1/PD-L1*制剂抑**联合其他药物、双特异性抗体、疫苗和肿瘤内异质性、过继性T细胞治疗[ACT])在转移性CRC中的作用。此外,免疫疗法在CRC辅助治疗和新辅助治疗中的作用也在探索中。
总结
CRC是一种异质性疾病,其免疫学基础日益为人们所熟知。尽管大多数肿瘤不会对目前的PD-1/PD-L1靶向免疫疗法产生反应,但高达20%的患者伴有MSI,而MSI是一个可从ICIs治疗中获益的明确的标志物,因而,FDA批准抗PD-1药物(帕博利珠单抗、纳武利尤单抗)或抗PD-1/抗CTLA4组合(纳武利尤单抗+伊匹木单抗)用于mCRC的治疗。鉴于抗PD-1单抗和抗PD-1/抗CTLA4联合治疗有效率和毒性发生率不同,因此,应根据患者的表现和对高缓解率的需要对患者进行个体化使用。目前的数据表明,在一线环境中使用ICIs对缓解率和生存率有明显的影响,而且在新辅助治疗中显示了有希望的活性。针对MSI-H/MMRd和MSS CRC,目前正在进行和未来将要进行的探索ICIs和其他免疫疗法在辅助/新辅助治疗以及晚期CRC中作用的试验,构成了一个快速扩大的研究领域,令人期待。