DC细胞
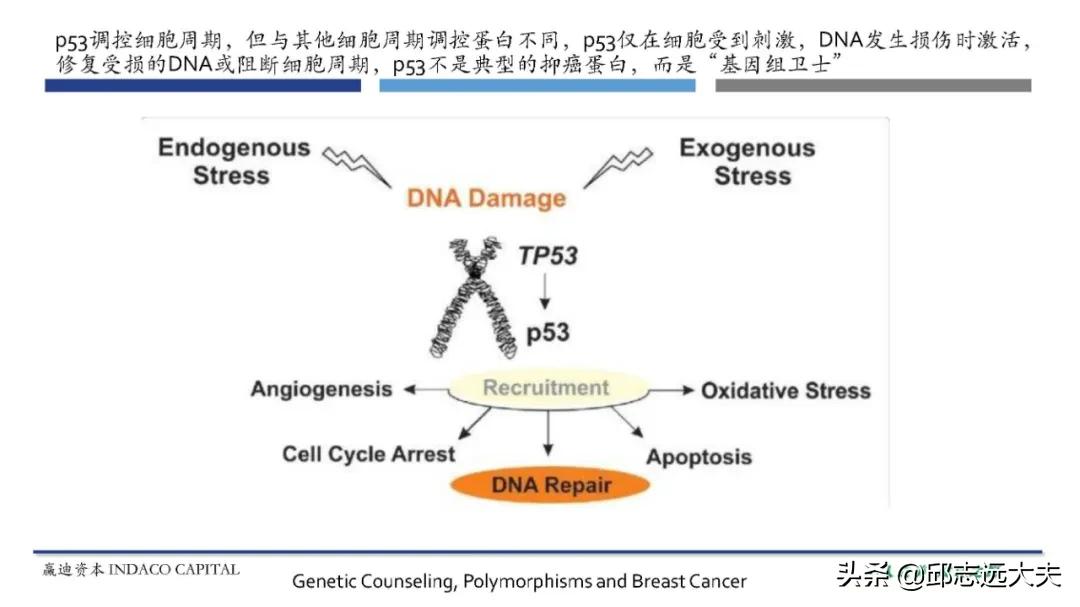
P53作为“基因组卫士”,在细胞的生长增殖中发挥重要的监控作用。当细胞受到外界压力,DNA发生损伤时,p53会被激活,启动DNA修复。当DNA受损严重时,p53会直接激活细胞周期阻滞,诱导细胞凋亡。癌症细胞往往携带大量基因突变,p53在肿瘤中起到抑癌作用。为了逃避p53的监控,50%的肿瘤都携带p53突变。突变的p53蛋白失去抑癌作用,无法控制肿瘤的生长。P53往往形成四聚体发挥作用,但四聚体如果包含了突变型p53,就可能导致整个四聚体失活,所以,在只有一个等位基因突变的情况下,突变型的p53也可以通过显性负效应作用,大大降低p53的活性。另外,某些p53突变,不仅使蛋白失去了正常功能,甚至还获得了新的能够促进肿瘤发生的功能,如促进血管生成、肿瘤迁移等。
P53突变位点贯穿整个基因,虽然50%肿瘤都携带p53突变,但靶向p53的疗法开发却非常困难。激活一个蛋白比抑制一个蛋白要困难很多,某些p53突变情势甚至没有完整的蛋白产生,而p53本身作为胞内蛋白,也没有供小分子结合的“活性口袋”。目前靶向p53的疗法主要包括靶向突变p53、合成致死和靶向MDM2-p53相互作用。其中,靶向突变p53的APR-246,可以恢复突变型p53的野生型功能,并且对多种p53突变有效,目前已在开展III期临床试验,前期数据显示,该分子的疗效和耐受性都很不错。MDM2是p53信号通路中的关键分子,该分子受p53诱导表达,起到负向调节p53的作用。抑制MDM2与p53之间的蛋白相互作用,可以提高p53的活性。罗氏该机制的小分子idasanutlin(RG7388)已经进展到III期临床,但今年6月宣布因为未达临床起点而终止该项目。虽然这个机制的药物研发还有许多困难,但仍有多项临床阶段的项目还在推进中。
早在2001年,人们就已经发现p53可以调控160多种基因,目前已发现多达几百种蛋白分子与p53之间有相互作用。P53作为关键分子,处在一个巨大且复杂的调控网络中,受到太多因素的影响。从生物学机制来讲,到底在何种条件下调控p53能达到抑制肿瘤的结果,并没有清晰的答案。同时,从成药性来讲,p53本身就是一个不可成药的靶点。但50%以上的突变率依然吸引着众多玩家在此领域不断耕耘。尽管暂时还未有突破性的结果,甚至频频遭受打击,但整个领域依然在艰难中前行。